Коррозия металла. почему возникает и как избежать
Содержание:
- Виды коррозии
- Виды
- Что мы узнали?
- Тест по теме
- Химические реакции
- Олово и цинк. «Опасные» и «безопасные покрытия
- Разрушительные процессы на меди
- Что нужно запомнить
- Оцинковка — не панацея
- Экономический ущерб от коррозии
- Коррозия в неэлектролитных жидкостях
- Виды коррозии бетона
- Методы и способы защиты металлов от коррозии
- Технический прогресс в развитии методов борьбы с коррозией
- Презентация на тему: » Примеры коррозии металлов.. Коррозия кузова автомобиля.» — Транскрипт:
Виды коррозии
Как уже говорилось, критериев классификация коррозионных процессов существует множество. Так, различают коррозию по виду распространения (сплошная, местная), по типу коррозионной среды (газовая, атмосферная, жидкостная, почвенная), по характеру механических воздействий (коррозионное растрескивание, явление Фреттинга, кавитационная коррозия) и так далее.
Но основным способом классификации коррозии, позволяющим наиболее полно объяснить все тонкости этого процесса, является классификация по механизму протекания.
По этому критерию различают два вида коррозии:
- химическую
- электрохимическую
Химическая коррозия
Химическая коррозия отличается от электрохимической тем, что протекает в средах, не проводящих электрический ток. Поэтому при такой коррозии разрушение металла не сопровождается возникновением электрического тока в системе. Это обычное окислительно-восстановительное взаимодействие металла с окружающей средой.
Наиболее типичным примером химической коррозии является газовая коррозия. Газовую коррозию еще называют высокотемпературной, поскольку обычно она протекает при повышенных температурах, когда возможность конденсации влаги на поверхности металла полностью исключена. К такому виду коррозии можно отнести, например, коррозию элементов электронагревателей или сопел ракетных двигателей.
Скорость химической коррозии зависит от температуры — при ее повышении коррозия ускоряется. Из-за этого, например, в процессе производства металлического проката, во все стороны от раскаленной массы разлетаются огненные брызги. Это с поверхности металла скалываются частички окалины.
Окалина — типичный продукт химической коррозии, — оксид, возникающий в результате взаимодействия раскаленного металла с кислородом воздуха.
Помимо кислорода и другие газы могут обладать сильными агрессивными свойствами по отношению к металлам. К таким газам относятся диоксид серы, фтор, хлор, сероводород. Так, например, алюминий и его сплавы, а также стали с высоким содержанием хрома (нержавеющие стали) устойчивы в атмосфере, которая содержит в качестве основного агрессивного агента кислород. Но картина кардинально меняется, если в атмосфере присутствует хлор.
В документации к некоторым антикоррозионным препаратам химическую коррозию иногда называют «сухой», а электрохимическую — «мокрой». Однако химическая коррозия может протекать и в жидкостях. Только в отличие от электрохимической коррозии эти жидкости — неэлектролиты (т.е. не проводящие электрический ток, например спирт, бензол, бензин, керосин).
Примером такой коррозии является коррозия железных деталей двигателя автомобиля. Присутствующая в бензине в качестве примесей сера взаимодействует с поверхностью детали, образуя сульфид железа. Сульфид железа очень хрупок и легко отслаивается, освобождая свежую поверхность для дальнейшего взаимодействия с серой. И так, слой за слоем, деталь постепенно разрушается.
Электрохимическая коррозия
Если химическая коррозия представляет собой не что иное, как простое окисление металла, то электрохимическая — это разрушение за счет гальванических процессов.
В отличие от химической, электрохимическая коррозия протекает в средах с хорошей электропроводностью и сопровождается возникновением тока. Для «запуска» электрохимической коррозии необходимы два условия: гальваническая пара и электролит.
В роли электролита выступает влага на поверхности металла (конденсат, дождевая вода и т.д.). Что такое гальваническая пара? Чтобы понять это, вернемся к ряду активности металлов.
Смотрим. Cлева расположены более активные металлы, справа — менее активные.
Если в контакт вступают два металла с различной активностью, они образуют гальваническую пару, и в присутствии электролита между ними возникает поток электронов, перетекающих от анодных участков к катодным. При этом более активный металл, являющийся анодом гальванопары, начинает корродировать, в то время как менее активный коррозии не подвергается.
Схема гальванического элемента
Для наглядности рассмотрим несколько простых примеров.
Допустим, стальной болт закреплен медной гайкой. Что будет корродировать, железо или медь? Смотрим в ряд активности. Железо более активно (стоит левее), а значит именно оно будет разрушаться в месте соединения.
Стальной болт — медная гайка (корродирует сталь)
А если гайка алюминиевая? Снова смотрим в ряд активности. Здесь картина меняется: уже алюминий (Al), как более активный металл, будет терять электроны и разрушаться.
Таким образом, контакт более активного «левого» металла с менее активным «правым» усиливает коррозию первого.
Виды
Коррозия может происходить в присутствии электролитов и неэлектролитов. Поэтому основными видами коррозии металлов по механизму возникновения являются:
- химическая – возникает в отсутствии электролита в сухой или влажной среде;
- электрохимическая – происходит в присутствии электролита.
Химическая коррозия связана с неэлектролитами – веществами, не проводящими электрический ток в растворах или расплавах. К неэлетролитам относятся многие простые неорганические (кислород, водород) и органические (эфир, бензол) вещества.
Химическая коррозия может происходить в присутствии газов (водорода, кислорода, хлора), органических кислот и солей. Молекулы металла соединяются с химическими элементами, и на металлической поверхности возникают плёнки – оксиды, сульфиды, гидриды. Внешне это заметно по изменению цвета. Железо, соединяясь с кислородом, образует Fe2O3 – оксид железа (III) – рыжую ржавчину.

Рис. 2. Оксид железа.
Если в расплаве или в растворе присутствуют вещества, проводящие электрический ток (электролиты), то появляется электрохимическая коррозия. Она возникает в присутствии солей, кислот, щелочей или при соприкосновении поверхностей двух металлов, между которыми находится влажная среда. Из-за разности окислительно-восстановительных потенциалов возникает гальванический элемент – источник электрического тока. Металл выступает в роли анода (восстановителя), электролит – катода (окислителя). Анод, отдавая электроны, окисляется или коррозирует.
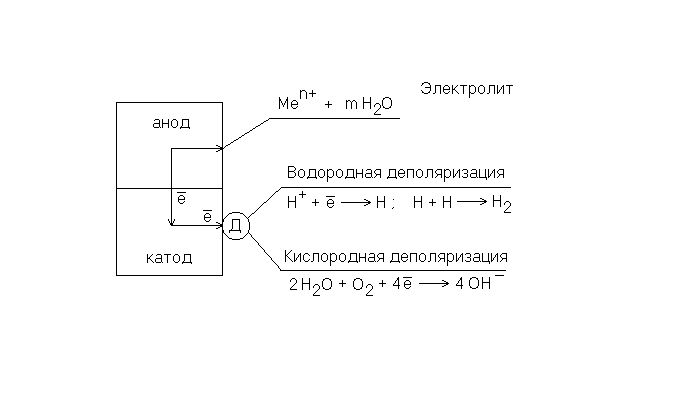
Рис. 3. Схема электрохимической коррозии.
Классификация коррозии может проводиться по другим признакам. По очагу поражения коррозия бывает:
- местной;
- сплошной;
- точечной.
Коррозия может происходить в разных средах:
- газовой (безводной);
- атмосферной (влажной);
- жидкостной;
- грунтовой;
- радиационной.
Соль ускоряет процесс ржавления, поэтому корабли быстрее ржавеют в морской, чем в пресной воде.
Что мы узнали?
Коррозия – окисление и разрушение металла под воздействием окружающей среды. Процесс окисления может происходить в присутствии или в отсутствии электролитов. Коррозия, возникающая без воздействия электролитов, называется химической. На поверхности металлов возникают оксиды, гидроксиды, соли. Под действием электролитов возникает электрохимическая коррозия. Окислению подвергается металл, выступающий в роли анода.
Тест по теме
-
Вопрос 1 из 5
Что происходит при коррозии?
- Окисление металла и восстановление корозионной среды
- Восстановление металла и окисление корозионной среды
- Окисление металла и коррозионной среды
- Восстановление металла и коррозионной среды
Начать тест(новая вкладка)
Химические реакции
Толстый слой ржавчины на звеньях цепи возле моста Золотые Ворота в Сан-Франциско. Цепь постоянно подвергается воздействию сырости и солёных брызг, вызывающих разрушение поверхности, растрескивание и шелушение металла.
Причины ржавления
Если железо, содержащее какие-либо добавки и примеси (например, углерод), находится в контакте с водой, кислородом или другим сильным окислителем и/или кислотой, то оно начинает ржаветь. Если при этом присутствует соль, например, имеется контакт с солёной водой, коррозия происходит быстрее в результате электрохимических реакций. Чистое железо относительно устойчиво к воздействию чистой воды и сухого кислорода. Как и у других металлов, например, у алюминия, плотно приставшее оксидное покрытие на железе (слой пассивации) защищает основную массу железа от дальнейшего окисления. Превращение же пассивирующего слоя оксида железа в ржавчину является результатом комбинированного действия двух реагентов, как правило, кислорода и воды. Другими разрушающими факторами являются диоксид серы и углекислый газ в воде. В этих агрессивных условиях образуются различные виды гидроксида железа. В отличие от оксидов железа, гидроксиды не защищают основную массу металла. Поскольку гидроксид формируется и отслаивается от поверхности, воздействию подвергается следующий слой железа, и процесс коррозии продолжается до тех пор, пока всё железо не будет уничтожено, или в системе закончится весь кислород, вода, диоксид углерода или диоксид серы.
Происходящие реакции
Покрытый ржавчиной и грязью болт. Заметна точечная коррозия и постепенная деформация поверхности, вызванная сильным окислением.
Ржавление железа — это электрохимический процесс, который начинается с переноса электронов от железа к кислороду. Скорость коррозии зависит от количества имеющейся воды, и ускоряется электролитами, о чём свидетельствуют последствия применения дорожной соли на коррозию автомобилей. Ключевой реакцией является восстановление кислорода:
- O2 + 4 e− + 2 H2O → 4 OH−
Поскольку при этом образуются гидроксид-анионы, этот процесс сильно зависит от присутствия кислоты. Действительно, коррозия большинства металлов кислородом ускоряется при понижении pH. Обеспечение электронов для вышеприведённой реакции происходит при окисления железа, которое может быть описано следующим образом:
- Fe → Fe2+ + 2 e−
Следующая окислительно-восстановительная реакция происходит в присутствии воды и имеет решающее значение для формирования ржавчины:
- 4 Fe2+ + O2 → 4 Fe3+ + 2 O2−
Кроме того, следующие многоступенчатые кислотно-щелочные реакции влияют на ход формирования ржавчины:
- Fe2+ + 2 H2O ⇌ Fe(OH)2 + 2 H+
- Fe3+ + 3 H2O ⇌ Fe(OH)3 + 3 H+
что приводит к следующим реакциям поддержания баланса дегидратации:
- Fe(OH)2 ⇌ FeO + H2O
- Fe(OH)3 ⇌ FeO(OH) + H2O
- 2 FeO(OH) ⇌ Fe2O3 + H2O
Из приведённых выше уравнений видно, что формирование продуктов коррозии обусловлено наличием воды и кислорода. С ограничением растворённого кислорода на передний план выдвигаются железо (II)-содержащие материалы, в том числе FeO и чёрный магнит (Fe3O4). Высокая концентрация кислорода благоприятна для материалов с трёхвалентным железом, с номинальной формулой Fe(OH)3-xOx/2. Характер коррозии меняется со временем, отражая медленные скорости реакций твёрдых тел.
Кроме того, эти сложные процессы зависят от присутствия других ионов, таких как Ca2+, которые служат в качестве электролита, и таким образом, ускоряют образование ржавчины, или в сочетании с гидроксидами и оксидами железа образуют различные осадки вида Ca-Fe-O-OH.
Более того, цвет ржавчины можно использовать для проверки наличия ионов Fe2+, которые меняют цвет ржавчины с жёлтого на синий.
Олово и цинк. «Опасные» и «безопасные покрытия
Возьмем еще пример. Допустим, кузовная панель покрыта оловом. Олово — очень стойкий к коррозии металл, кроме того, оно создает пассивный защитный слой, ограждая железо от взаимодействия с внешней средой. Значит, железо под слоем олова находится в целости и сохранности? Да, но только до тех пор, пока слой олова не получит повреждение.
А когда такое случается, между оловом и железом тут же возникает гальваническая пара, и железо, являющееся более активным металлом, под воздействием гальванического тока начнет корродировать.
Кстати, в народе до сих пор ходят легенды о якобы «вечных» луженых кузовах «Победы». Корни этой легенды таковы: ремонтируя аварийные машины, мастера использовали паяльные лампы для нагрева. И вдруг, ни с того ни с сего, из-под пламени горелки начинает «рекой» литься олово! Отсюда и пошла молва, что кузов «Победы» был полностью облужен.
На самом деле все гораздо прозаичнее. Штамповая оснастка тех лет была несовершенной, поэтому поверхности деталей получались неровными. Вдобавок тогдашние стали не годились для глубокой вытяжки, и образование морщин при штамповке стало обычным делом. Сваренный, но еще не окрашенный кузов приходилось долго готовить. Выпуклости сглаживали наждачными кругами, а вмятины заполняли оловяным припоем, особенно много которого было вблизи рамки ветрового стекла. Только и всего.
Ну, а так ли «вечен» луженый кузов, вы уже знаете: он вечен до первого хорошего удара острым камешком. А их на наших дорогах более чем достаточно.
А вот с цинком картина совсем другая. Здесь, можно сказать, мы бьем электрохимическую коррозию ее же оружием. Защищающий металл (цинк) в ряду напряжений стоит левее железа. А значит при повреждении будет разрушаться уже не сталь, а цинк. И только после того, как прокорродирует весь цинк, начнет разрушаться железо. Но, к счастью, корродирует он очень и очень медленно, сохраняя сталь на долгие годы.
а) Коррозия луженой стали: при повреждении покрытия разрушается сталь. б) Коррозия оцинкованной стали: при повреждении покрытия разрушается цинк, защищая от коррозии сталь.
Покрытия, выполненные из более активных металлов называются «безопасными«, а из менее активных — «опасными«. Безопасные покрытия, в частности оцинковка, давно и успешно применяются как способ защиты от коррозии автомобильных кузовов.
Почему именно цинк? Ведь помимо цинка в ряду активности относительно железа более активными являются еще несколько элементов. Здесь подвох вот в чем: чем дальше в ряду активности находятся друг от друга два металла, тем быстрее разрушение более активного (менее благородного). А это, соответственно, сокращает долговечность антикоррозионной защиты
Так что для автомобильных кузовов, где помимо хорошей защиты металла важно достичь и продолжительного срока действия этой защиты, оцинковка подходит как нельзя лучше. Тем более, что цинк доступен и недорог
Кстати, а что будет, если покрыть кузов, например, золотом? Во-первых, будет ох как дорого! Но даже если золото стало бы самым дешевым металлом, такого делать нельзя, поскольку оно окажет нашей «железке» плохую услугу.
Золото ведь стоит очень далеко от железа в ряду активности (дальше всего), и при малейшей царапине железо вскоре превратится в груду ржавчины, покрытую золотой пленкой.
Автомобильный кузов подвергается воздействию как химической, так электрохимической коррозии. Но главная роль все же отводится электрохимическим процессам.
Ведь, чего греха таить, гальванических пар в автомобильном кузове много: это и сварные швы, и контакты разнородных металлов, и посторонние включения в листовом прокате. Не хватает только электролита, чтобы «включить» эти гальванические элементы.
А электролит тоже найти легко — хотя бы влага, содержащаяся в атмосфере.
Кроме того, в реальных условиях эксплуатации оба вида коррозии усиливаются множеством других факторов. Поговорим о главных из них поподробнее.
Разрушительные процессы на меди
Медь считается достаточно стабильным металлом. Ее стабильность замечена в следующих средах:
- Атмосфера.
- Морская и пресная вода.
- Галогеновые среды со специальными условиями.
- В кислотах-неокислителях.
При этом медные конструкции отличаются нестабильностью в следующих условиях:
- При контакте с соединениями серы, а также с самой серой в чистом виде.
- При погружении в растворы солей-окислителей.
- В агрессивной воде.
Также часто встречается и атмосферная коррозия меди.
Ржавление железа
Еще один популярный элемент, который часто подвергается действию ржавчины — железо. Чаще всего железо подвергается разрушительным процессам в результате контакта с воздухом или кислотным раствором.
Что нужно запомнить
Оцинковка — не панацея
Сторонники отказа от дополнительной антикоррозионной обработки часто ссылаются на заводскую оцинковку: с ней, мол, никакая коррозия автомобилю не грозит. Но, как показали шведские ученые, это не совсем так.
Действительно, цинк может служить в качестве самостоятельной защиты, но только на ровных и плавных поверхностях, к тому же не подверженных механическим атакам. А на кромках, краях, стыках, а также местах, регулярно подвергающихся «обстрелу» песком и камнями, оцинковка перед коррозией пасует.
К тому же, далеко не у всех автомобилей кузова оцинкованы полностью. Чаще всего цинком покрыто лишь несколько панелей.
Ну и не нужно забывать, что цинк хоть и защищает сталь, но в процессе защиты неизбежно расходуется сам. Поэтому толщина цинкового «щита» со временем будет постепенно снижаться.
Так что легенды о долгожительстве оцинкованных кузовов правдивы лишь в тех случаях, когда цинк становится частью общей защиты, дополнением к регулярной дополнительной антикоррозионной обработке кузова.
Пора заканчивать, но на этом тема коррозии далеко не исчерпана. О борьбе с ней мы продолжим говорить в следующих статьях рубрики «Антикоррозионная защита».
Экономический ущерб от коррозии
Коррозия ухудшает работу трубопроводов.
Экономические потери от коррозии металлов огромны. В США по последним данным NACE, ущерб от коррозии и затраты на борьбу с ней составили 3,1 % от ВВП (276 млрд долларов). В Германии этот ущерб составил 2,8 % от ВВП. По оценкам специалистов различных стран эти потери в промышленно развитых странах составляют от 2 до 4 % валового национального продукта. При этом потери металла, включающие массу вышедших из строя металлических конструкций, изделий, оборудования, составляют от 10 до 20 % годового производства стали.
Обрушение Серебряного моста.
Ржавчина является одной из наиболее распространённых причин аварий мостов. Так как ржавчина имеет гораздо больший объём, чем исходная масса железа, её наращивание может привести к неравномерному прилеганию друг к другу конструкционных деталей. Это стало причиной разрушения моста через реку Мианус в 1983 году, когда подшипники кронштейна моста проржавели внутри. Три водителя погибли при падении в реку. Исследования показали, что сток дороги был перекрыт и не был почищен, а сточные воды проникли в опоры моста. Согласно исследованию Национального совета по безопасности на транспорте, разрушение моста было вызвано механической поломкой наружного кронштейна, удерживающего пролёт моста и его обоих штифтов. Ржавчина образовалась в подшипнике штифта. А так как её объём всегда гораздо больше, нежели исходная стальная деталь, это привело к неравномерному прилеганию друг к другу частей конструкции. В случае с мостом, ржавая масса отодвинула внутренний кронштейн от конца штифта, скрепляющего между собой наружный и внутренний кронштейны. (При этом возникло усилие, превышающее проектные пределы для зажимов, удерживающих штифты!) Из-за этого вся масса пролёта переместилась на внешний кронштейн. Эта дополнительная нагрузка на него вызвала усталостную трещину в штифте. Когда два тяжелых грузовика въехали в данную секцию моста, штифты окончательно вышли из строя, и пролёт моста упал в реку…
15 декабря 1967 года Серебряный мост, соединяющий Пойнт Плезант, штат Западная Виргиния, и Канауга, штат Огайо, неожиданно рухнул в реку Огайо. В момент обрушения 37 автомобилей двигались по мосту, и 31 из них упали вместе с мостом. Сорок шесть человек погибли, и девять серьёзно пострадали. Помимо человеческих жертв и травм, был разрушен основной транспортный путь между Западной Виргинией и Огайо. Причиной обрушения стала коррозия.
Мост Кинзу в Пенсильвании был разрушен в 2003 году от торнадо прежде всего потому, что центральные основные болты проржавели, существенно снизив его устойчивость.
Коррозия в неэлектролитных жидкостях
Общие сведения
К жидким неэлектропроводным средам (а точнее, неэлектролитным жидкостям) можно отнести такие органические вещества, к примеру:
- Керосин.
- Бензол.
- Бензин.
- Хлороформ.
- Нефть.
- Спирты.
- Фенол.
- Тетрахлорид углерода.
Еще к таким жидкостям причисляют малое количество жидкостей неорганического типа, к примеру, жидкий бром и сера, которая расплавлена. При этом следует отметить, что растворители органического типа сами по себе не будут вступать в реакцию с металлами, но, при наличие маленького объема примесей появляется интенсивный процесс взаимодействий. Скорость коррозии увеличивают находящиеся в нефти элементов с содержанием серы.
Также, для усиления коррозийных процессов нужны высокие температуры. Влага будет интенсифицировать развитие коррозии по электромеханическому принципу. Еще одним фактором быстрого коррозийного развития – бром в жидком виде. При нормальной температуре он особенно разрушительно будет воздействовать на высокоуглеродистые стали, титан и алюминий. Менее существенно воздействие брома на никель и железо, а самую большую устойчивость к жидкому типу брома будут показывать тантал, свинец, платина и серебро.
Расплавленная сера будет вступать в агрессивные реакции практически со всеми металлами, и в первую очередь с оловом, свинцом и медью. На углеродистые марки титан и стали сера будет влиять меньше, а еще практически полностью разрушает алюминий. Защитные действия для металлических конструкций, которые находятся в неэлектропроводных средах жидкого типа, проводят добавлением устойчивым к определенной среде металлом (к примеру, сталей с большим содержанием хрома). Еще используются особые защитные покрытия (к примеру, в среде, где есть много серы, применяют алюминиевые покрытия).
Способы защиты от коррозии
Способы борьбы с коррозией будут включать в себя:
- Обработку главного металла защитным слоем (например, нанесение лакокрасочного материала).
- Применение ингибиторов (арсенитов или хроматов).
- Внедрение материалов, которые устойчивые к коррозийным процессам.
Подбор определенного материала будет зависеть от потенциальной эффективности (тут имеется виде финансовой и технологической) ее применения.
Современные принципы по защите металла от химической коррозии металла будут основаны на следующих методиках:
- Улучшение споротивляемости химического типа. Себя смогли успешно зарекомендовать устойчивые материалы (стекло, высокополимерный пластик и керамика).
- Изоляция материала от агрессивных сред.
- Уменьшение агрессивности технологической среды – в роли примеров таких действий можно выполнить нейтрализацию и удалить кислотность в коррозионой среде, а еще применять различные ингибиторы.
- Защита электрохимического типа (накладывание внешнего тока).
Указанные методики будут подразделяться на две группы:
- Повышение сопротивляемости химического типа и изолирование будет применяться до того, как металлическая конструкция запускается в использовании.
- Уменьшение агрессивности и защиты электрохимического типа применяется уже при применении изделий и металла. Использование обеих методик дает возможность внедрять новые защитные методы, и в результате защита будет обеспечиваться изменением эксплуатационных условий.
Одним из самых часто используемых методов защиты металла является антикоррозийное гальваническое покрытие, но это экономически нерентабельно при большой площади поверхности. Причина в больших тратах на процесс подготовки. Ведущее место среди методов по защите будет занимать покрытие металла лакокрасочным материалом.
И все-таки, окрашенная поверхность защищает металлы от процессов коррозии даже при локальном повреждении пленки, тогда как несовершенные покрытия гальванического типы способны даже ускорить коррозию.
Виды коррозии бетона
Бетон является крепким каменным строительным материалом, состоящим из цемента, наполнителя и связующих веществ. Так как этот материал эксплуатируется в условиях открытой окружающей среды, а также нередко в агрессивно-опасных средах, то он так же подвержен коррозийному износу.
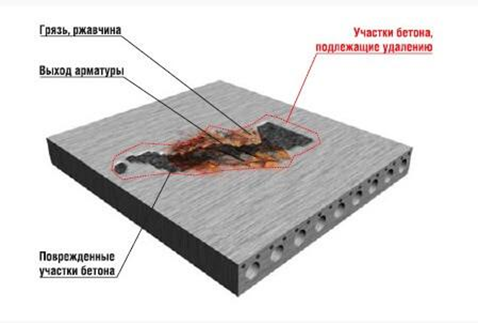
Схема коррозии на бетоне
Существует несколько видов бетонной коррозии:
- В результате взаимодействия с окружающей средой, на поверхности бетона могут образовываться легкорастворимые соли, которые при взаимодействии с внутренними компонентами материала приводят к его разрушению.
- Часто встречающаяся проблема – это разъединение составных частей цементного камня водой или вымывание гидроксида кальция, который образовывается в процессе такой реакции или ранее.
- В условиях окружающей среды, в состав бетона проникают вещества, которые имеют достаточно большой объем, в сравнении с исходными продуктами реакции, что приводит к механическим и химическим повреждениям целостности материала, далее эти участки под воздействием окружающей среды начинают коррозировать про принципу 1 или 2.
Методы и способы защиты металлов от коррозии
Вследствие того, что коррозийный процесс протекает на верхних слоях металла конструкции, то защита поверхности заключается в создании верхнего защитного слоя для изделия, который убирает следы коррозии на металле. Такими защитными покрытиями выступают вещества металлические и неметаллические.
Исходя из названия, металлические покрытия – это вещества, в основе которых металл. Например, чтобы защитить конструкцию из железа от коррозии на ее поверхность наносят слои цинка, меди или никеля.
Очистка труб от коррозии
Неметаллические покрытия – специальные вещества, наиболее широкая группа защитных соединений. Они изготавливаются в виде красок, эмалей, смазок, грунтовок, составов на битумной и битумно-полимерной основе и т.д.
Большая популярность неметаллических соединений в устранении следов коррозии заключается в их широком выборе, большом ценовом диапазоне, легкости изготовления и хороших защитных свойствах.
Наименьшую популярность приобрели химические покрытия из-за необходимости проводить сложные химические процессы:
- Оксидирование – образование оксидных пленок на поверхностях защищаемых деталей.
- Азотирование – насыщение верхних слоев материала азотом.
- Цементация – реакция, при которой верхние слои соединяются с углеродом и т.д.
Также при коррозии металлов существуют способы защиты, при которых на этапе сплавления металлов в них вводят специальные соединения, которые смогут повысить коррозийную устойчивость будущего материала.
Большую группу защиты представляют способы электрохимической и протекторной защиты.
Электрохимическая защита состоит в процессе преобразования продуктов коррозии в среде электролитов с помощью проводящего электрического тока. Постоянный ток присоединяется к катоду (защищаемому материалу), а в качестве анода выступает проводящий металлический источник, который при своем разрушении защищает объект от ржавчины.
Электрохимическая защита от коррозии
Протекторная защита протекает по такому же принципу, однако вместе металлического связующего изделия выступают специальные изделия – протекторы, которые выступают в роли анода. В результате протекающей реакции, протектор разрушается, защищая катод (конструкцию из металла).
Таким образом, хоть коррозия является необратимым процессом, но на данный момент люди научились эффективно замедлять ее губительное воздействие.
Технический прогресс в развитии методов борьбы с коррозией
Так как коррозионные потери металла составляют астрономическую сумму, технический прогресс продолжает предлагать новые методы борьбы с ней, по мере развития научных исследований и совершенствования аппаратного обеспечения . К ним относятся:
. К ним относятся:
- газотермическое напыление, образующее сверхтонкие защитные покрытия;
- термодиффузионные покрытия, создающие прочную поверхностную защиту;
- кадмирование, обеспечивающее защиту стали в морской воде.
Рост промышленного производства происходит с постоянным увеличением выпуска металлических изделий. Электрохимическая коррозия, вне зависимости от исторической эпохи, представляет постоянную угрозу огромному объему конструкций и ответственных сооружений. Поэтому создание новых методов и средств борьбы — одна из задач исследований технического прогресса.
Презентация на тему: » Примеры коррозии металлов.. Коррозия кузова автомобиля.» — Транскрипт:
1
Примеры коррозии металлов.
2
Коррозия кузова автомобиля
3
Коррозия весов
4
Ржавление железа на гараже
5
Коррозия корабля
6
Коррозия в доме
7
Коррозия моста.
8
Девиз урока Чтобы уметь бороться с коррозией, надо всё узнать о ней Академик Несмеянов
9
Понятие коррозии. Коррозия (от лат. corrodere — разъедать)- это самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды
10
Коррозия металлов Химическая Электрохимическая Происходит в не проводящей Происходит в токопроводящей электрический ток среде. Такой вид среде (в электролите) с коррозии проявляется в случае возникновением внутри системы взаимодействия металлов с сухими электрического тока. Условия газами или жидкостями – для электрохимической неэлектролитами. коррозии: 1) контакт двух (бензином, керосином и др.) металлов; 2) наличие электролита. Электро- химическая Химическая
11
Химическая коррозия. Химическая коррозия- это разрушение металла в результате химического взаимодействия его с окружающей средой без возникновения электрического тока. Например, образование окалины при взаимодействии материалов на основе железа при высокой температуре с кислородом. 4Fe+ 3O 2 2Fe 2 O 3
12
Уравнение реакции 4Fe+ 3O2 2Fe2O3
13
Электрохимическая коррозия. Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие контакта двух металлов и электролита как, например, при ржавлении железа во влажной атмосфере
14
Электрохимическая коррозия
15
Электрохимическая коррозия.
17
Способы борьбы с коррозией. Защита от коррозии конструкционных материалов в агрессивных средах основана на: 1) повышении коррозионной стойкости самого материала; 2) снижении агрессивной среды (ингибиторы) ; 3) предотвращении контакта материала со средой с помощью изолирующего покрытия ; 4) создание контакта с более активным металлом — протектором
18
Способы защиты от коррозии
19
Электрохимические методы защиты. Протекторная защита К защищаемой металлической конструкции присоединяют кусок более активного металла (протектор), который служит анодом и разрушается в присутствии электролита
20
Применение легированных сплавов. Они содержат специальные добавки: хром, никель, которые при высокой температуре на поверхности металла образуют устойчивый оксидный слой. Известны легированные стали – «нержавейки», из которых изготавливают предметы домашнего обихода, детали машин, инструменты..
21
Скульптура «Рабочий и колхозница» (нержавеющая сталь) Скульптор Вера Мухина
22
Ингибиторы коррозии В некоторых случаях пигменты красок выполняют роль ингибиторов коррозии. К числу таких пигментов относятся хроматы стронция, свинца и цинка. Ингибиторы- это вещества способные в малых количествах замедлять протекание химических процессов или останавливать их.
23
Применение ингибиторов. Специальная обработка электролита или другой среды: введение ингибиторов — веществ, замедляющих коррозию.
24
Заменители коррозирующих металлов Один из способов защиты от коррозии основывается на разработке новых материалов, обладающих более высокой коррозионной стойкостью. Постоянно ведутся поиски заменителей коррозирующих металлов. Пластмассы, керамика, стекло, резина, асбест и бетон более устойчивы к воздействию окружающей среды, однако по многим другим свойствам они уступают металлам, которые по- прежнему служат основными конструкционными материалами.
25
Изделия из железа. Железная колонна в Дели.
26
Колосс Родосский- 32 метра
27
Эйфелева башня (время строительства – ) Густав Эйфель — архитектор
28
Царь-пушка Царь-пушка Царь-колокол














